Intracellulaire infecties
Een geavanceerde analyse van bloedcellen op de
aanwezigheid en activiteit van verborgen pathogenen
Intracellulaire infecties
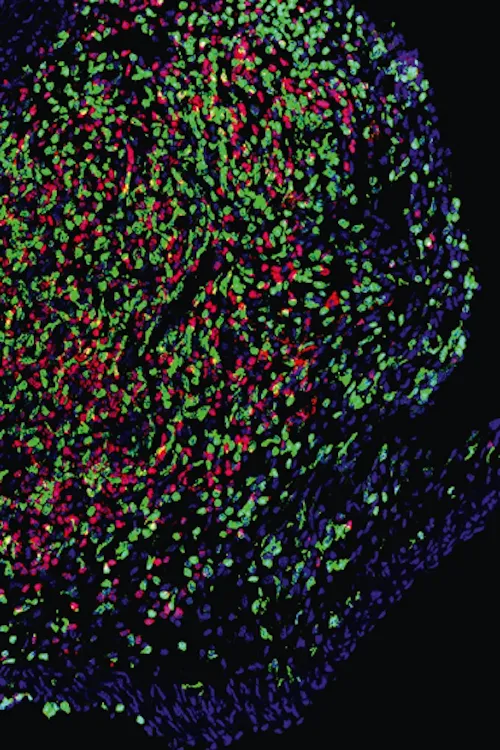
Biocoherence werkt samen met een geavanceerd laboratorium die een nieuwe gecombineerde analytische aanpak heeft ontwikkeld: Het in situ gebruik van fluorescent gelabelde DNA-probes en morfometrie in bloedcellen. Deze aanpak is gepatenteerd en blijkt in de praktijk zeer goed te werken. Uniek is dat naast de aanwezigheid van de ziekteverwerker, ook de metabole activiteit in de cellen wordt weergegeven. Wanneer de activiteit 0% is, betekent dit dat de pathogeen niet actief is, bij 100% is de pathogeen zeer actief.
CELL WALL DEFICIENT BACTERIA (CWBD) – ONZICHTBAAR VOOR HET IMMUUNSYSTEEM
Chronische infecties die lang blijven aanhouden
Bacteriën, schimmels en virussen kunnen een groot aantal ontstekingsreacties veroorzaken die worden gekenmerkt door traditionele ontstekingsparameters zoals koorts, roodheid, pijn, zwelling, vermoeidheid en functieverlies. Jarenlang bestond het beeld dat deze pathogenen met o.a. antibiotica worden behandeld, en hiermee de infecties kunnen worden onderdrukt.
Naast de bekende infecties blijken echter veel ziekteverwekkers ook in staat chronische intracellulaire infecties te veroorzaken. Uit de medische literatuur blijkt dat chronische ziektebeelden, maar vooral de daaruit voortvloeiende “post-infectieuze syndromen” gezien de impact op de kwaliteit van leven van veel groter belang zijn dan oorspronkelijk werd aangenomen. Deze intracellulaire infecties kunnen maanden of later aan het licht komen zodat ze niet in verband worden gebracht met de eerdere oorspronkelijk infectie. Deze late reacties op een eerdere infectie worden verantwoordelijk geacht voor een aanzienlijk aantal ziektebeelden, die dan ook een sterk auto-immuun aspect kennen.
DE STANDAARD DIAGNOSTIEK EN INTERVENTIE IS NIET TOEREIKEND
Een analyse die uitstijgt boven de standaard PCR
Naast het feit dat CWDB’s geen klassieke symptomen veroorzaken (en dus niet zichtbaar voor een medisch practicus) zijn ze eveneens moeilijk te diagnosticeren met traditionele methoden zoals:
GERICHTE INTERVENTIES INZETTEN
Aanwezigheid en activiteit van de pathogeen
Met deze analyse is het niet alleen mogelijk om een belangrijke diagnostische stap te zetten maar ook ontstaat zo de mogelijkheid om objectief het effect van een interventie die gericht is op de eliminatie van intracellulaire pathogenen, te monitoren, zowel in termen van de omvang van de infectie als de activiteit van het pathogeen.
De analyse wordt aangeboden aan therapeuten die actief zijn in de complementaire zorg. Zij kunnen (eventueel met behulp van ondersteuning van Biocoherence Nederland) de uitslag vertalen naar een interventie strategie. Deze strategie is gebaseerd op een wetenschappelijke interpretatie van de type interleukines en andere biomarkers naar een voedings- en supplement aanpak die deze stoffen kunnen onderdrukken of de vorming ervan kan voorkomen.
Een therapeut ontvangt een uitgebreide rapportage en wordt u door ons getraind in de interpretatie.
Vraag de Intracellulaire Infectie Analyse eenvoudig aan
De Intracellulaire Infectie Analyse kan worden aangevraagd door therapeuten die wanneer ze bij ons zijn geregistreerd, deze analyse via onze webshop kunnen bestellen. Wij verzorgen het contact met het lab, de cliënt kan via een prik-poli in zijn omgeving bloed laten prikken. De rapportage wordt door ons verzorgd en klaargezet in het platform My Health of separaat beschikbaar gesteld.